Кислоты - электролиты, при диссоциации которых из положительных ионов образуются только ионы H + :
HNO 3 ↔ H + + NO 3 — ;
CH 3 COOH↔ H + +CH 3 COO — .
Все кислоты классифицируют на неорганические и органические (карбоновые), которые также имеют свои собственные (внутренние) классификации.
При нормальных условияхзначительное количество неорганических кислот существуют в жидком состоянии, некоторые - в твёрдом состоянии (H 3 PO 4 , H 3 BO 3).
Органические кислоты с числом атомов углерода до 3 представляют собой легкоподвижные бесцветные жидкости с характерным резким запахом; кислоты с 4-9 атомами углерода — маслянистые жидкости с неприятным запахом, а кислоты с большим количеством атомов углерода— твёрдые вещества, нерастворимые в воде.
Химические формулы кислот
Химические формулы кислот рассмотрим на примере нескольких представителей (как неорганических, так и органических): хлороводородной кислоте -HCl, серной кислоте - H 2 SO 4 , фосфорной кислоте — H 3 PO 4 , уксусной кислоте - CH 3 COOH и бензойной кислоте - C 6 H 5 COOH. Химическая формула показывает качественный и количественный состав молекулы (сколько и каких атомов входит в конкретное соединение) По химической формуле можно вычислить молекулярную массу кислот (Ar(H) = 1 а.е.м., Ar(Cl) = 35,5 а.е.м., Ar(P) = 31 а.е.м., Ar(O) = 16 а.е.м., Ar(S) = 32 а.е.м., Ar(C) = 12 а.е.м.):
Mr(HCl) = Ar(H) + Ar(Cl);
Mr(HCl) = 1 + 35,5 = 36,5.
Mr(H 2 SO 4) = 2×Ar(H) + Ar(S) + 4×Ar(O);
Mr(H 2 SO 4) = 2×1 + 32 + 4×16 = 2 + 32 + 64 = 98.
Mr(H 3 PO 4) = 3×Ar(H) + Ar(P) + 4×Ar(O);
Mr(H 3 PO 4) = 3×1 + 31 + 4×16 = 3 + 31 + 64 = 98.
Mr(CH 3 COOH) = 3×Ar(С) + 4×Ar(H) + 2×Ar(O);
Mr(CH 3 COOH) = 3×12 + 4×1 + 2×16 = 36 + 4 + 32 = 72.
Mr(C 6 H 5 COOH) = 7×Ar(C) + 6×Ar(H) + 2×Ar(O);
Mr(C 6 H 5 COOH) = 7×12 + 6×1 + 2×16 = 84 + 6 + 32 = 122.
Структурные (графические) формулы кислот
Структурная (графическая) формула вещества является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы. Укажем структурные формулы каждого из вышеуказанных соединений:
Рис. 1. Структурная формула хлороводородной кислоты.

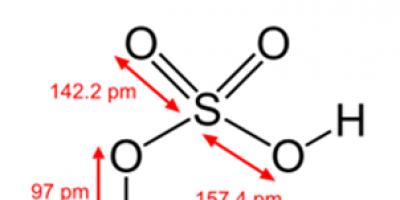
Рис. 2. Структурная формула серной кислоты.

Рис. 3. Структурная формула фосфорной кислоты.

Рис. 4. Структурная формула уксусной кислоты.

Рис. 5. Структурная формула бензойной кислоты.
Ионные формулы
Все неорганические кислоты являются электролитами, т.е. способны диссоциировать в водном растворе на ионы:
HCl ↔ H + + Cl — ;
H 2 SO 4 ↔ 2H + + SO 4 2- ;
H 3 PO 4 ↔ 3H + + PO 4 3- .
Примеры решения задач
ПРИМЕР 1
| Задание | При полном сгорании 6 г органического вещества образовалось 8,8 г оксида углерода (IV) и 3,6 г воды. Определите молекулярную формулу сожженного вещества, если известно, что его молярная масса равна 180 г/моль. |
| Решение | Составим схему реакции сгорания органического соединения обозначив количество атомов углерода, водорода и кислорода за «x», «у»и «z» соответственно:
C x H y O z + O z →CO 2 + H 2 O. Определим массы элементов, входящих в состав этого вещества. Значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: Ar(C) = 12 а.е.м., Ar(H) = 1 а.е.м., Ar(O) = 16 а.е.м. m(C) = n(C)×M(C) = n(CO 2)×M(C) = ×M(C); m(H) = n(H)×M(H) = 2×n(H 2 O)×M(H) = ×M(H); Рассчитаем молярные массы углекислого газа и воды. Как известно, молярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (M = Mr): M(CO 2) = Ar(C) + 2×Ar(O) = 12+ 2×16 = 12 + 32 = 44 г/моль; M(H 2 O) = 2×Ar(H) + Ar(O) = 2×1+ 16 = 2 + 16 = 18 г/моль. m(C) = ×12 = 2,4 г; m(H) = 2×3,6 / 18 ×1= 0,4 г. m(O) = m(C x H y O z) - m(C) - m(H) = 6 - 2,4 - 0,4 = 3,2 г. Определим химическую формулу соединения: x:y:z = m(C)/Ar(C) : m(H)/Ar(H) : m(O)/Ar(O); x:y:z= 2,4/12:0,4/1:3,2/16; x:y:z= 0,2: 0,4: 0,2 = 1: 2: 1. Значит простейшая формула соединения CH 2 Oи молярную массу 30 г/моль . Чтобы найти истинную формулу органического соединения найдем отношение истинной и полученной молярных масс: M substance / M(CH 2 O) = 180 / 30 = 6. Значит индексы атомов углерода, водорода и кислорода должны быть в 6 раз выше, т.е. формула вещества будет иметь вид C 6 H 12 O 6 . Это глюкоза или фруктоза. |
| Ответ | C 6 H 12 O 6 |
ПРИМЕР 2
| Задание | Выведите простейшую формулу соединения, в котором массовая доля фосфора составляет 43,66%, а массовая доля кислорода - 56,34%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле:
ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов фосфора в молекуле через «х», а число атомов кислорода через «у» Найдем соответствующие относительные атомные массы элементов фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(P) = 31; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y = ω(P)/Ar(P) : ω (O)/Ar(O); x:y = 43,66/31: 56,34/16; x:y: = 1,4: 3,5 = 1: 2,5 = 2: 5. Значит простейшая формула соединения фосфора и кислорода имеет вид P 2 O 5 . Это оксид фосфора (V). |
| Ответ | P 2 O 5 |
| Формула кислоты | Название кислоты | Название соли | Соответствующий оксид |
| HCl | Соляная | Хлориды | ---- |
| HI | Йодоводородная | Иодиды | ---- |
| HBr | Бромоводородная | Бромиды | ---- |
| HF | Плавиковая | Фториды | ---- |
| HNO 3 | Азотная | Нитраты | N 2 O 5 |
| H 2 SO 4 | Серная | Сульфаты | SO 3 |
| H 2 SO 3 | Сернистая | Сульфиты | SO 2 |
| H 2 S | Сероводородная | Сульфиды | ---- |
| H 2 CO 3 | Угольная | Карбонаты | CO 2 |
| H 2 SiO 3 | Кремниевая | Силикаты | SiO 2 |
| HNO 2 | Азотистая | Нитриты | N 2 O 3 |
| H 3 PO 4 | Фосфорная | Фосфаты | P 2 O 5 |
| H 3 PO 3 | Фосфористая | Фосфиты | P 2 O 3 |
| H 2 CrO 4 | Хромовая | Хроматы | CrO 3 |
| H 2 Cr 2 O 7 | Двухромовая | Бихроматы | CrO 3 |
| HMnO 4 | Марганцовая | Перманганаты | Mn 2 O 7 |
| HClO 4 | Хлорная | Перхлораты | Cl 2 O 7 |
Кислоты в лаборатории можно получить:
1) при растворении кислотных оксидов в воде:
N 2 O 5 + H 2 O → 2HNO 3 ;
CrO 3 + H 2 O → H 2 CrO 4 ;
2) при взаимодействии солей с сильными кислотами:
Na 2 SiO 3 + 2HCl → H 2 SiO 3 ¯ + 2NaCl;
Pb(NO 3) 2 + 2HCl → PbCl 2 ¯ + 2HNO 3 .
Кислоты взаимодействуют с металлами, основаниями, основными и амфотерными оксидами, амфотерными гидроксидами и солями:
Zn + 2HCl → ZnCl 2 + H 2 ;
Cu + 4HNO 3 (концентр.) → Cu(NO 3) 2 + 2NO 2 + 2H 2 O;
H 2 SO 4 + Ca(OH) 2 → CaSO 4 ¯ + 2H 2 O;
2HBr + MgO → MgBr 2 + H 2 O;
6HI + Al 2 O 3 → 2AlBr 3 + 3H 2 O;
H 2 SO 4 + Zn(OH) 2 → ZnSO 4 + 2H 2 O;
AgNO 3 + HCl → AgCl¯ + HNO 3 .
Обычно кислоты взаимодействуют только с теми металлами, которые в электрохимическом ряду напряжения стоят до водорода, при этом выделяется свободный водород. С малоактивными металлами (в электрохимическом ряду напряжения стоят после водорода) такие кислоты не взаимодействуют. Кислоты, являющиеся сильными окислителями (азотная, концентрированная серная), реагируют со всеми металлами, за исключением благородных (золото, платина), но при этом выделяется не водород, а вода и оксид, например, SO 2 или NO 2 .
Солью называют продукт замещения водорода в кислоте на металл.
Все соли делятся на:
средние – NaCl, K 2 CO 3 , KMnO 4 , Ca 3 (PO 4) 2 и др.;
кислые – NaHCO 3 , KH 2 PO 4 ;
основные – CuOHCl, Fe(OH) 2 NO 3 .
Средней солью называется продукт полного замещения ионов водорода в молекуле кислоты атомами металла.
Кислые соли содержат атомы водорода, способные участвовать в химических обменных реакциях. В кислых солях произошло неполное замещение атомов водорода атомами металла.
Основные соли – это продукт неполного замещения гидроксо-групп оснований многовалентных металлов кислотными остатками. Основные соли всегда содержат гидроксогруппу.
Средние соли получают взаимодействием:
1) кислоты и основания:
NaOH + HCl → NaCl + H 2 O;
2) кислоты и основного оксида:
H 2 SO 4 + CaO → CaSO 4 ¯ + H 2 O;
3) кислотного оксида и основания:
SO 2 + 2KOH → K 2 SO 3 + H 2 O;
4) кислотного и основного оксидов:
MgO + CO 2 → MgCO 3 ;
5) металла с кислотой:
Fe + 6HNO 3 (концентр.) → Fe(NO 3) 3 + 3NO 2 + 3H 2 O;
6) двух солей:
AgNO 3 + KCl → AgCl¯ + KNO 3 ;
7) соли и кислоты:
Na 2 SiO 3 + 2HCl → 2NaCl + H 2 SiO 3 ¯;
8) соли и щелочи:
CuSO 4 + 2CsOH → Cu(OH) 2 ¯ + Cs 2 SO 4 .
Кислые соли получают:
1) при нейтрализации многоосновных кислот щелочью в избытке кислоты:
H 3 PO 4 + NaOH → NaH 2 PO 4 + H 2 O;
2) при взаимодействии средних солей с кислотами:
СaCO 3 + H 2 CO 3 → Ca(HCO 3) 2 ;
3) при гидролизе солей, образованных слабой кислотой:
Na 2 S + H 2 O → NaHS + NaOH.
Основные соли получают:
1) при реакции между основанием многовалентного металла и кислотой в избытке основания:
Cu(OH) 2 + HCl → CuOHCl + H 2 O;
2) при взаимодействии средних солей со щелочами:
СuCl 2 + KOH → CuOHCl + KCl;
3) при гидролизе средних солей, образованных слабыми основаниями:
AlCl 3 +H 2 O → AlOHCl 2 + HCl.
Соли могут взаимодействовать с кислотами, щелочами, другими солями, с водой (реакция гидролиза):
2H 3 PO 4 + 3Ca(NO 3) 2 → Ca 3 (PO 4) 2 ¯ + 6HNO 3 ;
FeCl 3 + 3NaOH → Fe(OH) 3 ¯ + 3NaCl;
Na 2 S + NiCl 2 → NiS¯ + 2NaCl.
В любом случае реакция ионного обмена идет до конца только тогда, когда образуется малорастворимое, газообразное или слабо диссоциирующее соединение.
Кроме того, соли могут взаимодействовать с металлами при условии, что металл более активный (имеет более отрицательный электродный потенциал), чем металл, входящий в состав соли:
Fe + CuSO 4 → FeSO 4 + Cu.
Для солей также характерны реакции разложения:
BaCO 3 → BaO + CO 2 ;
2KClO 3 → 2KCl + 3O 2 .
Лабораторная работа №1
ПОЛУЧЕНИЕ И СВОЙСТВА
ОСНОВАНИЙ, КИСЛОТ И СОЛЕЙ
Опыт 1. Получение щелочей.
1.1. Взаимодействие металла с водой.
В кристаллизатор или фарфоровую чашечку налейте дистиллированной воды (примерно 1/2 сосуда). Получите у преподавателя кусочек металлического натрия, предварительно подсушенного фильтровальной бумагой. Бросьте кусочек натрия в кристаллизатор с водой. По окончании реакции добавьте несколько капель фенолфталеина. Отметьте наблюдаемые явления, составьте уравнение реакции. Назовите полученное соединение, запишите его структурную формулу.
1.2. Взаимодействие оксида металла с водой.
В пробирку налейте дистиллированной воды (1/3 пробирки) и поместите в нее комочек CaO, тщательно перемешайте, добавьте 1 – 2 капли фенолфталеина. Отметьте наблюдаемые явления, напишите уравнение реакции. Назовите полученное соединение, дайте его структурную формулу.
Рассмотрим наиболее часто встречающиеся в учебной литературе формулы кислот:
Легко заметить, что объединяет все формулы кислот наличие атомов водорода (H), стоящего на первом месте в формуле.
Определение валентности кислотного остатка
Из приведённого списка видно, что количество этих атомов может отличаться. Кислоты, в составе которых есть всего один атом водорода, называют одноосновными (азотная, соляная и другие). Серная, угольная, кремниевая кислоты — двухосновные, так как в их формулах по два атома H. Молекула трёхосновной фосфорной кислоты содержит три водородных атома.
Таким образом, количество H в формуле характеризует основность кислоты.
Тот атом, или группа атомов, которые записаны после водорода, называют кислотными остатками. Например, в сероводородной кислоте остаток состоит из одного атома — S, а в фосфорной, сернистой и многих других — из двух, причём один из них обязательно кислород (O). По этому признаку все кислоты делят на кислородсодержащие и бескислородные.
Каждый кислотный остаток обладает определённой валентностью. Она равна количеству атомов Н в молекуле этой кислоты. Валентность остатка HCl равна единице, так как это одноосновная кислота. Такую же валентность имеют остатки азотной, хлорной, азотистой кислот. Валентность остатка серной кислоты (SO 4) равна двум, так как атомов водорода в ее формуле два. Трехвалентен остаток фосфорной кислоты.
Кислотные остатки — анионы
Помимо валентности, кислотные остатки обладают зарядами и являются анионами. Их заряды указаны в таблице растворимости: CO 3 2− , S 2− , Cl − и так далее. Обратите внимание: заряд кислотного остатка численно совпадает с его валентностью. Например, в кремниевой кислоте, формула которой H 2 SiO 3 , кислотный остаток SiO 3 имеет валентность, равную II, и заряд 2-. Таким образом, зная заряд кислотного остатка, легко определить его валентность и наоборот.
Подведём итог. Кислотами — соединения, образованные атомами водорода и кислотными остатками. С точки зрения теории электролитической диссоциации можно дать другое определение: кислоты — электролиты, в растворах и расплавах которых присутствуют катионы водорода и анионы кислотных остатков.
Подсказки
Химические формулы кислот, как правило, заучивают наизусть, как и их названия. Если вы забыли, сколько атомов водорода в той или иной формуле, но знаете, как выглядит ее кислотный остаток, на помощь вам придёт таблица растворимости. Заряд остатка совпадает по модулю с валентностью, а та — с количеством H. К примеру, вы помните, что остаток угольной кислоты — CO 3 . По таблице растворимости определяете, что его заряд 2-, значит, он двухвалентен, то есть угольная кислота имеет формулу H 2 CO 3 .
Часто возникает путаница с формулами серной и сернистой, а также азотной и азотистой кислот. Здесь тоже есть один момент, облегчающий запоминание: название той кислоты из пары, в которой атомов кислорода больше, заканчивается на -ная (серная, азотная). Кислота с меньшим количеством атомов кислорода в формуле, имеет название, заканчивающееся на -истая (сернистая, азотистая).
Однако эти подсказки помогут лишь в том случае, если формулы кислот вам знакомы. Повторим их ещё раз.
Кислоты - сложные вещества, состоящие из одного или нескольких атомов водорода, способных замещаться на атома металлов, и кислотных остатков.
Классификация кислот
1. По числу атомов водорода: число атомов водорода (n ) определяет основность кислот:
n = 1 одноосновная
n = 2 двухосновная
n = 3 трехосновная
2. По составу:
а) Таблица кислород содержащих кислот, кислотных остатков и соответствующих кислотных оксидов:
|
Кислота (Н n А) |
Кислотный остаток (А) |
Соответствующий кислотный оксид |
|
H 2 SO 4 серная |
SO 4 (II) сульфат |
SO 3 оксид серы (VI ) |
|
HNO 3 азотная |
NO 3 (I) нитрат |
N 2 O 5 оксид азота (V ) |
|
HMnO 4 марганцевая |
MnO 4 (I) перманганат |
Mn 2 O 7 оксид марганца (VII ) |
|
H 2 SO 3 сернистая |
SO 3 (II) сульфит |
SO 2 оксид серы (IV ) |
|
H 3 PO 4 ортофосфорная |
PO 4 (III) ортофосфат |
P 2 O 5 оксид фосфора (V ) |
|
HNO 2 азотистая |
NO 2 (I) нитрит |
N 2 O 3 оксид азота (III ) |
|
H 2 CO 3 угольная |
CO 3 (II) карбонат |
CO 2 оксид углерода (IV ) |
|
H 2 SiO 3 кремниевая |
SiO 3 (II) силикат |
SiO 2 оксид кремния (IV) |
|
НСlO хлорноватистая |
СlO (I) гипохлорит |
С l 2 O оксид хлора (I) |
|
НСlO 2 хлористая |
СlO 2 (I) хлорит |
С l 2 O 3 оксид хлора (III) |
|
НСlO 3 хлорноватая |
СlO 3 (I) хлорат |
С l 2 O 5 оксид хлора (V) |
|
НСlO 4 хлорная |
СlO 4 (I) перхлорат |
С l 2 O 7 оксид хлора (VII) |
б) Таблица бескислородных кислот
|
Кислота (Н n А) |
Кислотный остаток (А) |
|
HCl соляная, хлороводородная |
Cl (I ) хлорид |
|
H 2 S сероводородная |
S (II ) сульфид |
|
HBr бромоводородная |
Br (I ) бромид |
|
HI йодоводородная |
I (I ) йодид |
|
HF фтороводородная,плавиковая |
F (I ) фторид |
Физические свойства кислот
Многие кислоты, например серная, азотная, соляная – это бесцветные жидкости. известны также твёрдые кислоты: ортофосфорная, метафосфорная HPO 3 , борная H 3 BO 3 . Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H 2 SiO 3 . Растворы кислот имеют кислый вкус. Так, например, многим плодам придают кислый вкус содержащиеся в них кислоты. Отсюда названия кислот: лимонная, яблочная и т.д.
Способы получения кислот
|
бескислородные |
кислородсодержащие |
|
HCl, HBr, HI, HF, H 2 S |
HNO 3 , H 2 SO 4 и другие |
|
ПОЛУЧЕНИЕ |
|
|
1. Прямое взаимодействие неметаллов H 2 + Cl 2 = 2 HCl |
1. Кислотный оксид + вода = кислота SO 3 + H 2 O = H 2 SO 4 |
|
2. Реакция обмена между солью и менее летучей кислотой 2 NaCl (тв .) + H 2 SO 4 (конц .) = Na 2 SO 4 + 2HCl |
|
Химические свойства кислот
1. Изменяют окраску индикаторов
|
Название индикатора |
Нейтральная среда |
Кислая среда |
|
Лакмус |
Фиолетовый |
Красный |
|
Фенолфталеин |
Бесцветный |
Бесцветный |
|
Метилоранж |
Оранжевый |
Красный |
|
Универсальная индикаторная бумага |
Оранжевая |
Красная |
2.Реагируют с металлами в ряду активности до H 2
(искл. HNO 3 –азотная кислота)
Видео "Взаимодействие кислот с металлами"
Ме + КИСЛОТА =СОЛЬ + H 2 (р. замещения)
Zn + 2 HCl = ZnCl 2 + H 2
3. С основными (амфотерными) оксидами – оксидами металлов
Видео "Взаимодействие оксидов металлов с кислотами"
Ме х О у + КИСЛОТА= СОЛЬ + Н 2 О (р. обмена)
4. Реагируют с основаниями – реакция нейтрализации
КИСЛОТА + ОСНОВАНИЕ= СОЛЬ+ H 2 O (р. обмена)
H 3 PO 4 + 3 NaOH = Na 3 PO 4 + 3 H 2 O
5. Реагируют с солями слабых, летучих кислот - если образуется кислота, выпадающая в осадок или выделяется газ:
2 NaCl (тв .) + H 2 SO 4 (конц .) = Na 2 SO 4 + 2HCl ( р . обмена )
Видео "Взаимодействие кислот с солями"
6. Разложение кислородсодержащих кислот при нагревании
(искл. H 2 SO 4 ; H 3 PO 4 )
КИСЛОТА = КИСЛОТНЫЙ ОКСИД + ВОДА (р. разложения)
Запомните! Неустойчивые кислоты (угольная и сернистая) – разлагаются на газ и воду :
H 2 CO 3 ↔ H 2 O + CO 2
H 2 SO 3 ↔ H 2 O + SO 2
Сероводородная кислота в продуктах выделяется в виде газа:
СаS + 2HCl = H 2 S + Ca Cl 2
ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
№1. Распределите химические формулы кислот в таблицу. Дайте им названия:
LiOH , Mn 2 O 7 , CaO , Na 3 PO 4 , H 2 S , MnO , Fe (OH ) 3 , Cr 2 O 3 ,HI , HClO 4 , HBr , CaCl 2 , Na 2 O , HCl , H 2 SO 4 , HNO 3 , HMnO 4 , Ca (OH ) 2 , SiO 2 , Кислоты
Бес-кисло-
родные
Кислород- содержащие
растворимые
нераст-воримые
одно-
основные
двух-основные
трёх-основные
№2. Составьте уравнения реакций:
Ca + HCl
Na + H 2 SO 4
Al + H 2 S
Ca
+ H 3 PO 4
Назовите продукты реакции.
№3. Составьте уравнения реакций, назовите продукты:
Na 2 O + H 2 CO 3
ZnO + HCl
CaO + HNO 3
Fe 2 O 3 + H 2 SO 4
№4. Составьте уравнения реакций взаимодействия кислот с основаниями и солями:
KOH + HNO 3
NaOH + H 2 SO 3
Ca(OH) 2 + H 2 S
Al(OH) 3 + HF
HCl + Na 2 SiO 3
H 2 SO 4 + K 2 CO 3
HNO 3 + CaCO 3
Назовите продукты реакции.
ТРЕНАЖЁРЫ
Тренажёр №1. "Формулы и названия кислот"
Тренажёр №2. " Установление соответствия: формула кислоты - формула оксида"
Техника безопасности - Оказание первой помощи при попадании кислот на кожу
Техника безопасности -